 |
 |
| 第1章 疾患・臨床研究の実際 |
 |
 |
|
 |
概説 |
|
| 1. | 遺伝子治療の臨床研究の実際 |
| 1.1. | 要旨 |
| 1.2. | はじめに |
| 2. | 遺伝子治療の対象疾患ならびにターゲット細胞 |
|
|
| 3. | 遺伝子治療の実際とその問題点 |
| 4. | わが国での遺伝子治療の臨床研究の体制とその間題点 |
|
| |
 |
各論-遺伝病 |
|
| 1. | 総論 |
| 1.1. | 遺伝病の発症機構 |
| 1.2. | 遺伝病の治療 |
| 1.3. | 遺伝子病の治療の現状 |
| 1.3.1. | 代謝の是正 |
| 1.3.2. | 酵素補充療法 |
| 1.3.3. | 細胞または臓器移植 |
| 1.4. | 遺伝子病治療の将来 |
| 2. | 単一因子性疾患 |
| 2.1. | アミノ酸代謝異常 |
| 2.1.1. | はじめに |
| 2.1.2. | フェニルケトン尿症 |
| 2.2. | アンモニア代謝異常症 |
| 2.2.1. | アンモニア代謝と尿素サイクル |
| 2.2.2. | アンモニア代謝異常症の臨床像 |
| 2.2.3. | 尿素サイクルを構成する酵素の異常症 |
| 2.2.4. | その他の原因により高アンモニア血症を来す遺伝性疾患 |
| 2.2.5. | 0TC欠損症のヒトへの応用研究 |
| 2.2.6. | おわりに |
| 2.3. | リソソーム病-ゴーシェ病 |
| 2.3.1. | はじめに |
| 2.3.2. | ゴーシェ病の欠損遺伝子 |
| 2.3.3. | ゴーシェ病の治療 |
| 2.3.4. | ゴーシェ病の遺伝子治療 |
| 2.3.5. | おわりに |
| 2.4. | リソソーム病-ニーマンピック病 |
| 2.4.1. | はじめに |
| 2.4.2. | NPD-A型およびB型 |
| 2.4.3. | NPD-C型(NPC) |
| 2.5. | リソソーム病-ムコ多糖症 |
| 2.5.1. | はじめに |
| 2.5.2. | cross-correctionについて |
| 2.5.3. |  型 型 |
| 2.5.4. |  型 型 |
| 2.5.5. |  型 型 |
| 2.5.6. | 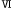 型 型 |
| 2.5.7. | 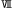 型 型 |
| 2.5.8. | おわりに |
| 2.6. | 免疫不全症侯群-ADA欠損症の遺伝子治療 |
| 2.6.1. | はじめに |
| 2.6.2. | ADA欠損症の病態とその治療法 |
| 2.6.3. | 海外におけるADA遺伝子治療 |
| 2.6.4. | 日本におけるADA遺伝子治療 |
| 2.6.5. | おわりに |
| 2.7. | 免疫不全症候群-慢性肉芽腫症CGD |
| 2.7.1. | 慢性肉芽腹症CGD(chronic granulomatous disease) |
| 2.7.2. | スーパーオキシド産生機序 |
| 2.7.3. | CGDの確定診断と病型分類 |
| 2.7.4. | CGD患者の遺伝子異常 |
| 2.7.5. | 本邦におけるCGD患者 |
| 2.7.6. | 治療法と成績 |
| 2.7.7. | 遺伝子導入発現による回復 |
| 2.7.8. | CGDの遺伝子治療 |
| 2.7.9. | CGDの遺伝子治療の将来 |
| 2.8. | 血液疾患に対する遺伝子治療Fanconi's Anemia(Fanconi貧血) |
| 2.8.1. | はじめに |
| 2.8.2. | Fanconi貧血の臨床的特徴と病態 |
| 2.8.3. | Fanconi貧血の病因遺伝子と遺伝子診断 |
| 2.8.4. | 遺伝子治療 |
| 2.9. | 神経疾患の遺伝子治療 |
| 2.9.1. | 神経疾患の遺伝子治療の考え方 |
| 2.9.2. | 遺伝子導入の方法(ex vivoとin vivoのアプローチ) |
| 2.9.3. | 神経疾患の遺伝子治療におけるウイルスベクターとその問題点 |
|
|
| 2.9.4. | パーキンソン病の遺伝子治療 |
| 2.9.5. | 遺伝子治療の将来への展望 |
| 2.10. | 嚢胞性線維症 |
| 2.10.1. | 嚢胞性線維症の臨床病態 |
| 2.10.2. | CFの分子生物学 |
| 2.10.3. | CFに対する遺伝子治療 |
| 2.10.4. | AdベクターによるCF遺伝子治療 |
| 2.10.5. | P1+LpベクターによるCF遺伝子治療 |
| 2.10.6. | AAVベクターによるCFの遺伝子治療 |
| 2.10.7. | CFの遺伝子治療についての将来への展望 |
| 2.11. | 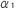 -アンチトリプシン欠損症 -アンチトリプシン欠損症 |
| 2.11.1. | 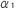 -アンチトリプシン欠損症の臨床病態 -アンチトリプシン欠損症の臨床病態 |
| 2.11.2. | 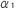 AT欠損症の分子病態 AT欠損症の分子病態 |
| 2.11.3. | 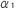 AT欠損症に対する治療 AT欠損症に対する治療 |
| 2.12. | 筋ジストロフィー |
| 2.12.1. | 分類 |
| 2.12.2. | 病因,病理 |
| 2.12.3. | 各論 |
| 2.12.4. | 治療(遺伝子治療の可能性) |
| 3. | 多因子性疾患 |
| 3.1. | 高脂血症 |
| 3.1.1. | はじめに |
| 3.1.2. | 家族性高コレステロール血症モデルとそれを用いた遺伝子治療との関連研究 |
| 3.1.3. | アポ蛋白異常モデルとそれを用いた遺伝子治療との関連研究 |
| 3.1.4. | リポ蛋白代謝関連酵素異常モデルとそれを用いた遺伝子治療との関連研究 |
| 3.1.5. | 複合病態モデルとそれを用いた遺伝子治療との関連研究 |
| 3.1.6. | 遺伝子導入による高脂血症治療の臨床応用の現況 |
| 3.1.7. | おわりに |
| 3.2. | 高血圧 |
| 3.2.1. | はじめに |
| 3.2.2. | 原因遺伝子解明への戦略 |
| 3.2.3. | 高血圧発症におけるアンジオテンシノーゲン(AGT)遺伝子の関与 |
| 3.2.4. | モデル動物による高血圧遺伝子探索の現状 |
| 3.2.5. | 遺伝子治療の可能性 |
| 3.2.6. | おわりに |
| 3.3. | 糖尿病 |
| 3.3.1. | はじめに |
| 3.3.2. | 多遺伝子性疾患としての糖尿病 |
| 3.3.3. | 多遺伝子性疾患の遺伝子解析 |
| 3.3.4. | 連鎖解析による疾患遺伝子座位の決定法 |
| 3.3.5. | 多遺伝子性疾患の連鎖解析における最近のアプローチ |
| 3.3.6. | おわりに |
| 3.4. | パーキンソン病 |
| 3.4.1. | パーキンソン病の原因 |
| 3.4.2. | 家族性パーキンソニズム |
| 3.4.3. | パーキンソン病治療の現状 |
| 3.4.4. | パーキンソン病の手術療法 |
| 3.4.5. | パーキンソン病の移植療法 |
| 3.4.6. | パーキンソン病の細胞保護療法 |
| 3.4.7. | パーキンソン病の遺伝子治療 |
| 3.4.8. | パーキンソン病遺伝子治療の将来 |
| 3.5. | 動脈硬化 |
| 3.5.1. | はじめに |
| 3.5.2. | 動脈硬化に対する遺伝子導入法の開発 |
| 3.5.3. | 閉塞性動脈硬化症に対する遺伝子治療 |
| 3.5.4. | 家族性高脂血症に対する遺伝子治療 |
| 3.5.5. | 心筋梗塞に対する遺伝子治療 |
| 3.5.6. | 高リボプロテイン(a)血症に対する遺伝子治療 |
| 3.5.7. | 動脈硬化に対する遺伝子治療の将来 |
|
| |
 |
各論-感染症 |
|
| 1. | 総論 |
| 1.1. | 感染症に対する遺伝子治療とは何か |
| 1.2. | 感染細胞攻撃戦略 |
| 1.2.1. | 直接攻撃戦略 |
| 1.2.2. | 免疫学的攻撃戦略 |
| 1.3. | 細胞内免疫戦略 |
| 1.3.1. | 核酸戦略 |
| 1.3.2. | 蛋白質戦略 |
| 1.4. | 展望 |
| 2. | HIV感染症 |
| 2.1. | はじめに |
| 2.2. | HIV感染症の臨床と病態 |
| 2.3. | HIV感染症の治療と問題点 |
| 2.4. | HIV感染症に対する遺伝子治療の可能性 |
| 2.4.1. | RNAによるHIV増殖抑制 |
| 2.4.2. | 蛋白によるHIV増殖抑制 |
| 2.4.3. | トキシン(毒素) |
| 2.5. | レトロベクターを用いた免疫強化(ワクチン療法)としての遺伝子治療 |
| 2.6. | おわりに |
| 3. | B型,C型肝炎 |
| 3.1. | B型肝炎 |
| 3.1.1. | 臨床的特徴 |
| 3.1.2. | B型肝炎ウイルス |
| 3.1.3. | 感染経路 |
| 3.1.4. | HBVと肝癌 |
| 3.1.5. | 予防・診断・治療 |
| 3.2. | C型肝炎 |
| 3.2.1. | 臨床的特徴 |
| 3.2.2. | C型肝炎ウイルス |
| 3.2.3. | 感染経路 |
| 3.2.4. | HCVと肝癌 |
| 3.2.5. | 予防・診断・治療 |
| 3.3. | 肝細胞癌の遺伝子治療 |
| 4. | EBウイルス感染症 |
| 4.1. | はじめに |
| 4.2. | 遺伝子治療の適応と考えられるEBV関連疾患とその戦略 |
|
|
| 4.2.1. | 遺伝子導入を伴う養子免疫療法 |
| 4.2.2. | 腫蕩組織への遺伝子導入 |
| 4.3. | おわりに |
| 5. | ヘルペスウイルス |
| 5.1. | ウイルスの性状と分類 |
| 5.2. | ウイルスの形態 |
| 5.2.1. | 核酸 |
| 5.2.2. | 蛋白 |
| 5.2.3. | リピッド |
| 5.3. | ウイルスの増殖 |
| 5.4. | 化学療法 |
| 5.5. | 潜伏感染 |
| 5.5.1. | 潜伏ウイルスの証明 |
| 5.5.2. | HSV感染の動物モデル |
| 5.5.3. | 潜伏の分子生物学 |
| 5.6. | 臨床ウイルス学 |
| 5.6.1. | 単純ヘルペスウイルス(HSV) |
| 5.6.2. | 水痘・帯状ヘルペスウイルス(VZV) |
| 5.6.3. | HHV-6およびHHV-7 |
| 5.6.4. | HHV-8 |
| 6. | サイトメガロウイルス |
| 6.1. | はじめに |
| 6.2. | ウイルス学的事項 |
| 6.2.1. | 分類 |
| 6.2.2. | ウイルスゲノム |
| 6.2.3. | ウイルス遺伝子 |
| 6.2.4. | ウイルスゲノムDNAの複製 |
| 6.2.5. | ウイルス粒子 |
| 6.2.6. | 糖蛋白 |
| 6.3. | 臨床的事項 |
| 6.4. | 診断 |
| 6.4.1. | ウイルス分離 |
| 6.4.2. | 迅速診断のためのウイルス抗原の検出 |
| 6.4.3. | 病理組織学的診断 |
| 6.4.4. | ウイルスゲノムの検出 |
| 6.5. | 治療 |
| 6.6. | おわりに |
|
| |
 |
各論-癌 |
|
| 1. | 総論 |
| 1.1. | はじめに |
| 1.2. | 悪性腫瘍の生物学的特徴 |
| 1.2.1. | 細胞増殖の制御 |
| 1.2.2. | 細胞死の制御 |
| 1.2.3. | 分化の制御 |
| 1.2.4. | 遺伝子不安定性 |
| 1.2.5. | 抗腫瘍免疫の修飾 |
| 1.3. | 悪性腫瘍に対する遺伝子治療の基本的戦略 |
| 1.3.1. | 薬剤感受性の増強(自殺遺伝子) |
| 1.3.2. | 免疫遺伝子治療 |
| 1.3.3. | 増殖抑制遺伝子の導入 |
| 1.3.4. | 腫瘍遺伝子の抑制 |
| 1.3.5. | 血管新生の抑制 |
| 1.3.6. | QOLの改善と目的とした治療 |
| 1.3.7. | その他の方法 |
| 1.4. | 悪性腫瘍に対する遺伝子治療の現状と今後 |
| 2. | 固形癌 |
| 2.1. | 脳腫瘍 |
| 2.1.1. | 脳腫瘍とは |
| 2.1.2. | 悪性グリオーマに対する遺伝子治療 |
| 2.1.3. | おわりに |
| 2.2. | 肺癌 |
| 2.2.1. | はじめに |
| 2.2.2. | 癌細胞に対する特異的免疫機構の増強 |
| 2.2.3. | 薬剤感受性遺伝子導入による癌細胞死の誘導 |
| 2.2.4. | 癌関連遺伝子の発現修飾による抗腫瘍効果 |
| 2.2.5. | アデノウイルスベクターによる肺癌細胞への遺伝子導入 |
| 2.2.6. | おわりに |
| 2.3. | 大腸癌 |
| 2.3.1. | はじめに |
| 2.3.2. | 大腸癌の遺伝子変化に対応する遺伝子治療法 |
| 2.3.3. | 標的自殺遺伝子治療 |
| 2.3.4. | おわりに |
| 2.4. | 卵巣癌 |
| 2.4.1. | 卵巣癌の遺伝子治療の背景 |
| 2.4.2. | 各卵巣癌遺伝子治療プロトコールの実際 |
| 2.4.3. | 卵巣癌遺伝子治療プロトコールの問題点 |
| 2.5. | 前立腺癌 |
| 2.5.1. | 前立腺癌について |
| 2.5.2. | 遺伝子治療について |
| 2.5.3. | 遺伝子導入法 |
| 2.5.4. | 前立腺癌に対する遺伝子治療 |
| 2.5.5. | 前立腺癌遺伝子治療の臨床研究の実際 |
| 2.5.6. | 今後の展望 |
| 2.6. | 腎癌 |
|
|
| 2.6.1. | はじめに |
| 2.6.2. | 腎癌について |
| 2.6.3. | 転移性腎癌に対する治療法の現況 |
| 2.6.4. | わが国における腎癌に対する遺伝子治療の現況 |
| 2.6.5. | 今後の展望 |
| 2.7. | メラノーマに対する遺伝子治療 |
| 2.7.1. | メラノーマの特徴 |
| 2.7.2. | 遺伝子導入による癌細胞傷害 |
| 2.7.3. | 癌細胞に対する免疫応答増強 |
| 2.7.4. | 今後の問題 |
| 2.8. | Neuroblastoma |
| 2.8.1. | はじめに |
| 2.8.2. | Neuroblastomaの細胞遺伝学的,細胞生物学的背景 |
| 2.8.3. | Neuroblastomaの遺伝子治療へ向けての考え方 |
| 2.8.4. | これまでの実験的試み |
| 2.8.5. | 将来の遺伝子治療のターゲット |
| 2.8.6. | おわりに |
| 2.9. | head&neck |
| 2.9.1. | はじめに |
| 2.9.2. | HSV-tk |
| 2.9.3. | p53 |
| 2.9.4. | IL-2 |
| 2.9.5. | IL-12 |
| 2.9.6. | p16INK4A,p21 |
| 2.9.7. | MnSOD |
| 2.9.8. | HLA-B7 |
| 2.9.9. | 上咽頭癌における遺伝子治療 |
| 3. | 血液・リンパの癌 |
| 3.1. | 総論 |
| 3.1.1. | 造血器 |
| 3.1.2. | 血液・リンパの癌(造血器腫瘍) |
| 3.1.3. | 造血器腫瘍に対する遺伝子治療 |
| 3.1.4. | 現状と今後 |
| 3.2. | ホジキン病(および悪性リンパ腫) |
| 3.2.1. | 悪性リンパ腫の分類 |
| 3.2.2. | 悪性リンパ腫に対する治療の現況 |
| 3.2.3. | ホジキン病・悪性リンパ腫に対する遺伝子治療 |
| 3.3. | 造血器悪性腫瘍(リンパ腫/白血病) |
| 3.3.1. | はじめに |
| 3.3.2. | 造血器悪性腫瘍の治療限界と治療法開発の方向性 |
| 3.3.3. | 遺伝子免疫療法 |
| 3.3.4. | 移植後再発白血病に対するドナーリンパ球輸注療法への応用 |
| 3.3.5. | おわりに |
|
| |
 |
各論-循環器 |
|
| 1. | 総論 |
| 1.1. | はじめに |
| 1.2. | 閉塞性動脈硬化症に対する遺伝子治療 |
| 1.3. | 心筋梗塞に対する遺伝子治療 |
| 1.4. | 再狭窄に対する遺伝子治療 |
| 1.5. | バイパス後再狭窄に対する遺伝子治療 |
| 1.6. | おわりに |
| 2. | 虚血性心疾患,とくに冠状動脈狭窄性病変に対する血管形成術後の再狭窄 |
|
|
| 2.1. | はじめに |
| 2.2. | 再狭窄の病因 |
| 2.3. | 再狭窄予防のための遺伝子治療 |
| 2.3.1. | 総論 |
| 2.3.2. | 各論 |
| 2.4. | おわりに |
|
| |
 |
各論-その他 |
|
| 1. | 自己免疫性疾患 |
| 1.1. | はじめに |
| 1.2. | 自己免疫疾患の治療戦略 |
| 1.3. | 自己免疫疾患治療における遺伝子療法の位置づけ |
| 1.4. | 自己免疫疾患治療における遺伝子療法の戦術 |
| 1.5. | 自己免疫疾患モデル動物を用いた遺伝子療法の例 |
| 1.6. | おわりに |
| 2. | アトピー |
| 2.1. | アトピー関連遺伝子 |
|
|
| 2.2. | アトピー疾患に対する遺伝子療法 |
| 2.3. | おわりに |
| 3. | 血管障害 |
| 3.1. | はじめに |
| 3.2. | 再狭窄に対する遺伝子治療 |
| 3.2.1. | 血管平滑筋細胞増殖抑制療法 |
| 3.2.2. | 内皮再生療法(リモデリング療法) |
| 3.3. | 冠動脈バイパスに対する遺伝子治療 |
| 3.4. | 血管疾患に対する遺伝子治療の将来 |
|
| |
| |
| 第2章 遺伝子治療概要 |
 |
 |
|
|
|
| 1. | はじめに |
| 2. | 遺伝子治療の歴史的背景 |
| 3. | 医学・医療への組換えDNA技術研究の効用 |
| 4. | 疾患遺伝子の同定と治療 |
|
|
| 5. | バイオテクノロジーと遺伝子治療: 新しい製薬企業の創製 |
| 6. | 医療経済への波及効果 |
|
| |
| |
| 第3章 導入技術 |
 |
 |
|
 |
総論 |
|
| 1. | 総説 |
| 1.1. | 遺伝子治療の利点 |
| 1.2. | 人体への遺伝子導入例 |
| 1.2.1. | 単一遺伝子病に対する遺伝子導入 |
| 1.2.2. | 癌治療と遺伝子導入 |
| 1.2.3. | エイズ治療における遺伝子導入 |
| 1.3. | 遺伝子導入の基礎 |
| 1.3.1. | 標識遺伝子 |
| 1.3.2. | 発現制御 |
| 1.3.3. | 安全性:発癌,感染防止 |
| 1.4. | トランスフェクション(遺伝子移入) |
| 1.4.1. | 物理的方法 |
| 1.4.2. | 化学的方法 |
| 1.4.3. | エンドサイトーシス法 |
| 1.5. | トランスダクション(遺伝子導入) |
| 1.6. | 目的遺伝子の相同組換え |
| 1.7. | おわりに |
| 2. | ベクター導入法 |
| 2.1. | ウイルスベクター |
| 2.1.1. | はじめに |
| 2.1.2. | レトロウイルスベクター |
| 2.1.3. | アデノウイルスベクター |
| 2.1.4. | アデノ随伴ウイルス(AAV)ベクター |
| 2.1.5. | おわりに |
| 2.2. | 非ウイルスベクター |
| 2.2.1. | DNAの細胞内導入と発現 |
| 2.2.2. | 培養細胞への遺伝子導入法 |
| 2.2.3. | 組織への遺伝子導入が可能な方法 |
| 2.2.4. | 非ウイルスベクターの将来 |
| 3. | 標的特異性-細胞特異的遺伝子導入法 |
| 3.1. | はじめに |
| 3.2. | 特定の細胞で遺伝子を発現させる方法(転写調節によるターゲッティング) |
|
|
| 3.3. | 特定の細胞に遺伝子を導入する方法(細胞ターゲッティング) |
| 3.3.1. | 遺伝子を直接局所に注入する方法(in situ遺伝子導入) |
| 3.3.2. | 標的細胞に親和性のあるベクターによる方法 |
| 3.4. | 2段階遺伝子導入による方法 |
| 3.5. | おわりに |
| 4. | 相同組換えによる遺伝子変異の修正 |
| 4.1. | はじめに |
| 4.1.1. | 相同組換え法のメリット |
| 4.1.2. | マウスの遺伝子ターゲッティングとの違い |
| 4.1.3. | c-DNA導入法との関係 |
| 4.1.4. | 本稿の内容 |
| 4.2. | 相同組換え |
| 4.2.1. | 相同組換えの機構 |
| 4.2.2. | 真核生物の相同組換え関連遺伝子産物 |
| 4.2.3. | 相同組換えの役割 |
| 4.3. | 非相同組換え |
| 4.3.1. | 定義 |
| 4.3.2. | DNA切断の再結合 |
| 4.4. | 相同組換えによって引き起こされる非相同組換え |
| 4.5. | ホモロジーの長さの影響 |
| 4.6. | ホモロジーの程度の影響 |
| 4.7. | DNA導入法,とくにウイルスの利用 |
| 4.7.1. | エレクトロポレーション |
| 4.7.2. | レトロウイルス |
| 4.7.3. | アデノウイルス |
| 4.8. | 効率上昇のための最近の試み |
| 4.8.1. | 三本鎖DNA |
| 4.8.2. | 短いDNA |
| 4.8.3. | DNA/RNAキメラ |
| 4.9. | 最近の研究の問題点 |
| 4.10. | おわりに |
|
| |
 |
各論 |
|
| 1. | ウイルスベクター |
| 1.1. | レトロウイルスの増殖サイクル |
| 1.1.1. | はじめに |
| 1.1.2. | レトロウイルスの構造 |
| 1.1.3. | レトロウイルスの増殖サイクルの概略 |
| 1.1.4. | 吸着 |
| 1.1.5. | 侵入 |
| 1.1.6. | 逆転写 |
| 1.1.7. | 宿主染色体への組込み |
| 1.1.8. | RNA合成 |
| 1.1.9. | 蛋白合成 |
| 1.1.10. | ウイルス粒子のアセンブリー・放出 |
| 1.1.11. | 成熟 |
| 1.1.12. | その他 |
| 1.1.13. | おわりに |
| 1.2. | レトロウイルスベクター |
| 1.2.1. | レトロウイルスベクターの特徴,利点と欠点 |
| 1.2.2. | レトロウイルスベクターの作製法ならびに利用法 |
| 1.2.3. | レトロウイルスベクターの宿主スペクトラム |
| 1.2.4. | おわりに |
| 1.3. | レトロウイルスベクターを使った遺伝子治療のプロトコール1 |
| 1.3.1. | はじめに |
| 1.3.2. | 造血幹細胞 |
| 1.3.3. | レトロウイルスベクターを用いて造血幹細胞に遺伝子導入するためのプロトコール |
| 1.3.4. | 造血幹細胞への遺伝子導入を高めるための工夫 |
| 1.3.5. | おわりに |
| 1.4. | レトロウイルスベクターを使った遺伝子治療のプロトコール2 |
| 1.4.1. | 遺伝子治療におけるレトロウイルスベクターの有用性 |
| 1.4.2. | レトロウイルスベクターの改良 |
| 1.4.3. | 実際の遺伝子治療に向けての基礎実験 |
| 1.4.4. | 今後の課題 |
| 1.5. | アデノウイルスの増殖サイクル |
| 1.5.1. | はじめに |
| 1.5.2. | アデノウイルスの細胞接着から核内侵入 |
| 1.5.3. | アデノウイルスの複製増幅 |
| 1.5.4. | 初期遺伝子 |
| 1.5.5. | 後期遺伝子 |
| 1.5.6. | アデノウイルスDNAの複製 |
| 1.5.7. | アデノウイルスの感染細胞 |
| 1.6. | アデノウイルスベクター |
| 1.6.1. | はじめに |
| 1.6.2. | ベクター素材としてのアデノウイルス |
| 1.6.3. | アデノウイルスベクター |
| 1.6.4. | 直接毒性と免疫反応 |
| 1.6.5. | 遺伝子治療研究への応用 |
| 1.6.6. | 次世代アデノウイルスベクターの展望 |
| 1.6.7. | おわりに |
| 1.7. | AAVの増殖サイクル |
| 1.7.1. | AAVの特徴 |
| 1.7.2. | AAVの増殖サイクル |
| 1.7.3. | Rep蛋白質 |
| 1.7.4. | AAVSl特異的組込み機構 |
| 1.8. | AAVベクター |
| 1.8.1. | はじめに |
| 1.8.2. | 一般的なAAVベクター作製法 |
| 1.8.3. | 導入効率を高める試み |
| 1.8.4. | AAVベクターの特徴 |
| 1.8.5. | AAVベクターによる遺伝子導入の実際 |
| 1.8.6. | おわりに |
| 1.9. | 単純ヘルペスウイルス(HSV)の増殖サイクル |
| 1.9.1. | ウイルス粒子とゲノムの構造 |
| 1.9.2. | 増殖機構 |
| 1.9.3. | 潜伏感染の分子機構 |
| 1.10. | HSVベクター |
| 1.10.1. | はじめに |
| 1.10.2. | HSV-1の構造 |
| 1.10.3. | HSV-1の増殖サイクル |
| 1.10.4. | HSV-1遺伝子発現 |
| 1.10.5. | HSV-1ベクター |
| 1.10.6. | 実際の使用 |
| 1.10.7. | おわりに |
|
|
| 1.11. | HIVの増殖サイクル |
| 1.11.1. | はじめに |
| 1.11.2. | HIVのウイルス粒子および遺伝子構造および増殖サイクルの概要 |
| 1.11.3. | CD4陽性細胞への吸着侵入 |
| 1.11.4. | 逆転写 |
| 1.11.5. | プレインテグレーション複合体の核内輸送 |
| 1.11.6. | インテグレーション |
| 1.11.7. | 転写およびスプライシング調節 |
| 1.11.8. | ウイルス蛋白のプロセッシング,アセンブリーから出芽まで |
| 1.11.9. | その他の遺伝子の増殖サイクルにおける役割 |
| 1.11.10. | おわりに |
| 1.12. | HIVベクター |
| 1.12.1. | はじめに |
| 1.12.2. | HIVベクターの作製法 |
| 1.12.3. | HIVベクターの特徴 |
| 1.12.4. | HIVベクターによるAIDSの遺伝子治療 |
| 1.12.5. | 非リンパ球への遺伝子導入 |
| 1.12.6. | おわりに |
| 1.13. | バキュロウイルスベクター |
| 1.13.1. | はじめに |
| 1.13.2. | 組換えウイルスの作製方法 |
| 1.13.3. | 哺乳動物細胞への遺伝子導入 |
| 1.13.4. | アデノウイルスベクターとの比較 |
| 1.13.5. | 遺伝子発現の持続と感染性ウイルスの消長 |
| 1.13.6. | 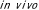 での発現 での発現 |
| 1.13.7. | T7 RNAポリメラーゼを発現する組換えバキュロウイルス |
| 1.13.8. | おわりに |
| 2. | リポソーム |
| 2.1. | カナオニックリポソーム |
| 2.1.1. | はじめに |
| 2.1.2. | カチオニックリポソームの調製法 |
| 2.1.3. | カチオニックリポソームの性状と遺伝子導入 |
| 2.2. | センダイウイルス(HVJ)の増殖サイクル |
| 2.2.1. | センダイウイルスの増殖サイクル |
| 2.2.2. | 非ウイルスベクターの構成成分としてのセンダイウイルスの特徴と問題点 |
| 2.2.3. | 組換えウイルスベクターとしてのセンダイウイルスの可能性と問題点 |
| 2.2.4. | おわりに |
| 2.3. | HVJリポソームベクター |
| 2.3.1. | はじめに |
| 2.3.2. | HVJ-リポソーム法の原理・特徴 |
| 2.3.3. | HVJ-カチオニックリポソーム,HVJ-AVE(artificial viral envelope)リポソーム |
| 2.3.4. | Epstein-Barr virus(EBV)レプリコンを用いた遺伝子発現期間の長期化の試み |
| 2.3.5. | 将来の展望 |
| 2.3.6. | HVJ-リポソームの作製プロトコール |
| 2.3.7. | HVJ-リポソームを用いた遺伝子治療研究の成果 |
| 3. | 直接DNA |
| 3.1. | gene gun |
| 3.1.1. | はじめに |
| 3.1.2. | 原理 |
| 3.1.3. | 準備するもの |
| 3.1.4. | プロトコール |
| 3.1.5. | 導入遺伝子の発現 |
| 3.2. | naked DNA |
| 3.2.1. | はじめに |
| 3.2.2. | おわりに |
| 4.. | イムノジーン法 |
| 4.1. | はじめに |
| 4.2. | イムノポーターの作製 |
| 4.3. | イムノジーンの作製 |
| 4.4. | イムノジーンのレセプターへの結合と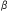 GAL遺伝子の核への移行 GAL遺伝子の核への移行 |
| 4.5. | イムノジーンによる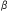 GAL遺伝子の発現 GAL遺伝子の発現 |
| 4.6. | イムノジーンによる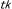 遺伝子の導入と殺細胞効果の誘発 遺伝子の導入と殺細胞効果の誘発 |
| 4.7. | イムノジーンによる担癌ヌードマウスの治療 |
| 4.8. | イムノジーン法の特徴 |
| 4.9. | イムノジーン法のさらなる改良点 |
| 4.10. | おわりに |
|
| |
| |
| 第4章 標的組織/細胞 |
 |
 |
|
 |
造血幹細胞 |
|
| 1. | はじめに |
| 2. | ヒトPHSCによる遺伝子治療の問題点 |
| 2.1. | ヒトPHSCへの遺伝子導入 |
| 2.2. | 導入遺伝子の長期発現 |
| 2.3. | 分化に伴う導入遺伝子の発現の変化 |
| 3. | マウスおよびヒト以外の霊長類を用いた遺伝子導入実験 |
| 3.1. | マウス |
| 3.2. | ヒト以外の霊長類 |
|
|
| 4. | PHSCを用いた遺伝子治療例 |
| 5. | 将来の遺伝子治療に向けて |
| 5.1. | ウイルスベクター |
| 5.2. | パッケージング細胞株 |
| 5.3. | ヒトPHSCの供給源 |
| 5.4. | ヒトPHSCの分離および濃縮法 |
| 5.5. | 遺伝子導入法 |
| 6. | おわりに |
|
| |
 |
末梢血細胞 |
|
| 1. | はじめに |
| 2. | 対象疾患 |
| 2.1. | ADA欠損症 |
| 2.2. | ウイルス感染症 |
|
|
| 2.3. | 癌 |
| 3. | 遺伝子治療のための末梢血T細胞の培養法 |
| 4. | おわりに |
|
| |
 |
筋肉細胞 |
|
| 1. | はじめに |
| 2. | 骨格筋細胞/組織に対する遺伝子導入の対象となる遺伝子 |
| 3. | 骨格筋培養細胞/組織に対する遺伝子導入法 |
| 3.1. | 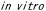 遺伝子導入法と 遺伝子導入法と 遺伝子導入法 遺伝子導入法 |
| 3.2. | ウイルスベクター |
| 3.2.1. | アデノウイルスベクター |
| 3.2.2. | レトロウイルスベクター |
| 3.2.3. | アデノ随伴ウイルス(AAV)ベクター |
| 3.2.4. | レンチウイルスベクター |
|
|
| 3.3. | 物理化学的方法 |
| 3.3.1. | plasmid DNAの直接導入法 |
| 3.3.2. | カチオン性脂質の利用 |
| 4. | 骨格筋細胞/組織に対する遺伝子導入における問題点とその対策 |
| 4.1. | 骨格筋細胞/組織に対する遺伝子の導入効率 |
| 4.2. | どのプロモーターを選択するのか |
| 4.3. | 投与経路 |
| 4.4. | 安全性 |
| 5. | 骨格筋に対する遺伝子導入の将来像 |
|
| |
 |
神経細胞 |
|
| 1. | はじめに |
| 2. | 神経細胞および神経組織の特徴 |
| 2.1. | 神経細胞 |
| 2.2. | 神経膠細胞 |
| 2.2.1. | アストロサイト |
| 2.2.2. | オリゴデンドログリア |
| 2.2.3. | ミクログリア |
| 3. | 神経系の培養 |
|
|
| 4. | ベクターについて |
| 5. | 神経疾患遺伝子治療実験の実際 |
| 5.1. | パーキンソン病 |
| 5.1.1. | ドーパミン生合成酵素遺伝子導入 |
| 5.1.2. | 神経栄養因子遺伝子導入 |
| 5.2. | 筋萎縮性側索硬化症(ALS) |
| 5.3. | アルツハイマー病 |
|
| |
 |
血管壁細胞 |
|
| 1. | はじめに |
| 2. | 遺伝子導入ベクター |
| 3. | 導入分子 |
|
|
| 4. | 導入分子の実際 |
| 5. | ベクター導入方法 |
| 6. | 遺伝子治療への展望 |
|
| |
 |
皮膚と遺伝子治療 |
|
| 1. | はじめに |
| 2. | 遺伝子導入法 |
| 3. | 遺伝子注入法 |
| 3.1. | マイクロインジェクション法 |
| 3.2. | エレクトロボレーション法 |
| 4. | レポーター遺伝子 |
|
|
| 5. | プロモーター |
| 5.1. | 先天性皮膚疾患 |
| 5.2. | 皮膚腫瘍 |
| 5.3. | その他 |
| 6. | おわりに |
|
| |
 |
肝細胞 |
|
| 1. | はじめに |
| 2. | 肝臓へ遺伝子を導入する方法 |
| 2.1. | 遺伝子を導入する方法/経路 |
| 2.2. | 遺伝子運搬体(ベクター) |
|
|
| 3. | 肝臓を標的とした遺伝子治療研究 |
| 3.1. | 原発性肝癌 |
| 3.2. | 転移性肝癌 |
| 4. | おわりに |
|
| |
 |
癌細胞 |
|
| 1. | はじめに |
| 2. | 腫瘍細胞への遺伝子導入 |
| 2.1. | ウイルスベクターの応用 |
| 2.2. | リポソームあるいは遺伝子銃 |
| 2.3. | トランスフェリン受容体を介した遺伝子導入 |
|
|
| 2.4. | EGF受容体を介した遺伝子導入 |
| 2.5. | リンパ球によるtargeting |
| 2.6. | 細胞特異的プロモーターによるtargeting |
| 2.7. | その他 |
| 3. | おわりに |
|
| |
 |
遺伝子導入細胞の選択・制御 |
|
| 1. | 選択遺伝子 |
| 1.1. | 選択遺伝子とは |
| 1.1.1. | 細胞選択の必要性 |
| 1.1.2. | 選択遺伝子の分類 |
| 1.2. | 各々の選択遺伝子 |
| 1.2.1. |  選択 選択 |
| 1.2.2. | 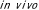 選択 選択 |
| 1.3. | おわりに |
| 2. | 抗癌剤耐性遺伝子 |
| 2.1. | はじめに |
| 2.2. | 造血幹細胞を標的としたex vivo遺伝子治療への抗癌剤耐性遺伝子の利用 |
| 2.3. | 抗癌剤多剤耐性遺伝子MDRl |
| 2.4. | 癌化学療法における骨髄抑制とその対策 |
| 2.5. | MDRl遺伝子治療の基礎および臨床研究 |
| 2.6. | 日本におけるMDRl遺伝子を用いた乳癌の遺伝子治療の臨床計画 |
|
|
| 2.7. | 他の抗癌剤耐性遺伝子 |
| 2.8. | MDRl遺伝子と第二の遺伝子を共発現させるレトロウイルスベクター |
| 2.9. | 慢性肉芽腫症の遺伝子治療への応用 |
| 2.10. | おわりに |
| 3. | 自殺遺伝子 |
| 3.1. | はじめに |
| 3.2. | VDEPT療法 |
| 3.2.1. | 機能発現 |
| 3.2.2. | Bystander効果 |
| 3.3. | 選択遺伝子/自殺遺伝子 |
| 3.4. | 大腸菌のシトシンデアミナーゼ |
| 3.5. | ジフテリア毒素遺伝子 |
| 3.6. | アポトーシス誘導遺伝子 |
| 3.7. | おわりに |
|
| |
| |
| 第5章 遺伝子の発現調節 |
 |
 |
|
 |
特異的遺伝子発現のメカニズム |
|
| 1. | 序論 |
| 1.1. | はじめに |
| 1.2. | 遺伝子発現の素過程 |
| 1.3. | RNA合成 |
| 2. | プロモーターと基本転写因子 |
| 2.1. | プロモーター |
| 2.2. | 基本転写因子 |
| 2.3. | 転写開始複合体形成と転写開始反応 |
| 2.4. | TBPとTAF |
| 2.5. | TFⅡHの酵素活性とDNA修復活性の共役 |
| 2.6. | ホロpolⅡ |
| 3. | エンハンサーと転写制御因子 |
| 3.1. | エンハンサーの発見 |
| 3.2. | エンハンサーの機能 |
| 3.3. | 転写制御因子とその構造 |
| 3.4. | 応答配列 |
| 4. | DNA上での制御シグナルの伝達 |
|
|
| 4.1. | 因子同士の接近および結合 |
| 4.2. | 転写メデイエーター |
| 4.3. | 転写効率が上昇する機構 |
| 4.4. | メデイエーターの関与するヒストンの化学修飾 |
| 4.5. | 細胞外刺激の受容と応答配列 |
| 5. | 転写制御因子の活性調節 |
| 5.1. | 化学修飾による変化 |
| 5.2. | 二量体形成反応 |
| 5.3. | 細胞外刺激の受容 |
| 5.4. | 転写の抑制 |
| 6. | 特異的転写を生み出す要因 |
| 6.1. | 特異的制御因子の発現および活性化 |
| 6.2. | 特異性が発揮されるその他の機構 |
| 6.3. | 基本転写因子の中にある特異性決定要因 |
| 7. | 特異的プロモーター〈特異的プロモーターとその選定の基準〉 |
|
| |
 |
転写調節因子 |
|
| 1. | HLH型転写因子 |
| 1.1. | クラスA |
| 1.2. | クラスB |
| 1.3. | クラスC |
| 1.4. | クラスD |
| 1.5. | クラスE |
| 2. | ホメオドメイン蛋白とホメオティック遺伝子群 |
| 2.1. | 脊椎動物の後脳の分節化 |
| 2.2. | ショウジョウバエの体節形成とホメオティック遺伝子群 |
| 2.3. | ホメオドメインとホメオボックス |
| 2.4. | 脊椎動物の後脳の分節化とホメオティック遺伝子群 |
| 2.5. | 前脳の部域特異化 |
| 2.6. | ホメオティック遺伝子群の発現制御機構 |
| 2.7. | ホメオティック遺伝子産物は抑制的または修飾的に作用する |
| 2.8. | ホメオティック遺伝子群の構造と並び方は進化の過程でなぜ保存されてきたのか |
| 2.9. | 脊椎動物の進化とホメオティック遺伝子群 |
| 2.10. | ホメオボックス遺伝子の突然変異と疾患 |
| 3. | LIM/ホメオドメイン型転写因子群 |
| 3.1. | LIM/ホメオドメイン型転写因子ファミリー |
| 3.2. | Islet-1遺伝子群とゼブラフィッシュ運動神経細胞の特異化 |
|
|
| 3.3. | LIM/ホメオドメイン型転写因子群とニワトリ胚運動神経細胞特異化 |
| 3.4. | LIM/ホメオドメイン蛋白におけるLIM領域の働き |
| 4. | からだづくりとHox遺伝子 |
| 4.1. | Hox遺伝子とHox群 |
| 4.2. | Hox遺伝子の発現と前後軸パターニングにおける役割 |
| 4.3. | 転写調節 |
| 5. | ZicとGli |
| 5.1. | はじめに |
| 5.2. | 構造 |
| 5.3. | 生物学的役割 |
| 5.3.1. | Zicファミリー |
| 5.3.2. | Gliファミリー |
| 5.4. | 疾病とのかかわり |
| 5.4.1. | Zicファミリー |
| 5.4.2. | Gliファミリー |
| 6. | CREB |
| 6.1. | はじめに |
| 6.2. | CREBによる細胞周期制御 |
| 6.3. | CREBと癌 |
| 6.4. | CREBと長期増強,記憶 |
| 6.5. | おわりに |
|
| |
 |
テトラサイクリンシステム |
|
| 1. | はじめに |
| 2. | 原理 |
| 2.1. | Tet-Offシステム |
| 2.2. | Tet-Onシステム |
| 3. | 手順 |
| 3.1. | 考察 |
| 3.2. | 注意 |
| 4. | 応用 |
| 4.1. | レトロウイルスベクター |
| 4.2. | アデノウイルスベクター |
|
|
| 4.2.1. | ベクター型-その1 |
| 4.2.2. | ベクター型-その2 |
| 4.3. | autoregulation |
| 4.4. | トランスジェニックマウスヘの応用 |
| 4.5. | パッケージ細胞の構築 |
| 5. | 問題点 |
| 5.1. | tightness/leakiness |
| 5.2. | Tet-On vs Tet-Off |
| 5.3. | nls-rtTAとnls-tTA |
| 6. | おわりに |
|
| |
 |
誘導・調節可能プロモーター(放射線感受性プロモーターEGR-1) |
|
| 1. | はじめに |
| 2. | 前初期反応遺伝子群(immediate-early genes) |
| 3. | 細胞増殖と放射線感受性遺伝子 |
| 4. | EGR-1プロモーター |
| 5. | EGR-1プロモーターの遺伝子治療への応用 |
|
|
| 6. | 特異的な腫瘍細胞の殺戮 |
| 7. | 放射性同位元素による発現調節 |
| 8. | ウイルスベクターでの発現検証 |
| 9. | 腫瘍細胞殺戮遺伝子の選択 |
| 10. | おわりに |
|
| |
 |
アンチセンス法による遺伝情報ノックアウト戦略法 |
|
| 1. | はじめに |
| 2. | アンチセンス核酸の分子設計 |
| 2.1. | 標的塩基配列の選択 |
| 2.2. | アンチセンスオリゴマーの長さの検討 |
| 2.3. | 標的配列の高次構造 |
| 2.4. | 分子設計の必要条件と実験法の開発 |
| 3. | 第二,三世代新規アンチセンス核酸化合物 |
| 3.1. | リン酸ジエステル結合の修飾法 |
| 3.2. | ヘテロサイクルの修飾法 |
| 3.3. | 糖の修飾法 |
| 3.4. | 核酸骨格を操作しない方法 |
| 4. | ヌクレアーゼ抵抗性 |
|
|
| 5. | 細胞膜透過性,ターゲッティング |
| 5.1. | オリゴマーはエンドサイトーシスで細胞内へ運ばれる |
| 5.2. | オリゴマー非特異的結合蛋白質 |
| 5.3. | オリゴマーの膜透過能の検討 |
| 5.4. | リポソームを利用したターゲッティング |
| 5.5. | オリゴマーの細胞内分布 |
| 6. | 送達システムの再評価 |
| 7. | 非アンチセンス効果 |
| 8. | 大量精製 |
| 9. | おわりに |
|
| |
 |
リボザイム技術 |
|
| 1. | はじめに |
| 2. | リボザイムの細胞内での発現 |
| 3. | 新規RNAモチーフであるマキシザイム |
| 4. | マキシザイムの効果的な利用法 |
|
|
| 5. | tRNA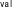 配列が付加したマキシザイム 配列が付加したマキシザイム |
| 6. | マキシザイムによる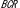 - -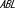 mRNAの発現抑制効果 mRNAの発現抑制効果 |
| 7. | おわりに |
|
| |
 |
単鎖抗体 |
|
| 1. | IgG抗体とは何か |
| 2. | 単鎖抗体とは何か |
| 3. | 単鎖抗体はどのようにして作製されるか |
| 4. | 作製上の注意と問題点 |
| 5. | 単鎖抗体の遺伝子治療への応用 |
|
|
| 5.1. | 抗癌 |
| 5.2. | 抗感染症 |
| 5.3. | 細胞内蛋白質輸送の阻害 |
| 5.4. | 組織特異的ベクターの作製 |
| 6. | おわりに |
|
| |
| |
| 第6章 安全性 |
 |
 |
|
 |
総論 |
|
| 1. | 概説 |
| 1.1. | はじめに |
| 1.2. | 遺伝子操作の安全性 |
| 1.3. | 遺伝子治療の安全性〈遺伝子治療の先進国〉 |
| 1.4. | 遺伝子治療臨床研究の承認過程 |
| 1.5. | 将来への展望と倫理上の問題点 |
| 1.5.1. | 生殖細胞への遺伝子治療への展望 |
| 1.5.2. | 将来に向けて |
| 2. | 安全性の実際-総論 |
|
|
| 2.1. | 安全性論議の背景 |
| 2.2. | 倫理的視点からの安全性の確保 |
| 2.3. | 技術的視点からの安全性の確保 |
| 2.3.1. | 生物学的な安全性を確保するための試験 |
| 2.3.2. | 体内動態試験 |
| 2.3.3. | 遺伝子治療用医薬品の製造上の安全性と品質の確保 |
| 2.3.4. | 遺伝子導入に際しての安全性の確保 |
|
| |
 |
各論 |
|
| 1. | ウイルスベクターの安全性 |
| 1.1. | はじめに |
| 1.2. | 非増殖性ウイルスベクターの安全性 |
| 1.2.1. | レトロウイルスベクターの安全性 |
| 1.2.2. | アデノウイルスベクターの安全性 |
| 1.2.3. | アデノ随伴ウイルス(AAV)ベクターの安全性 |
| 1.3. | 増殖性ウイルスベクターの安全性 |
| 1.3.1. | ワクシニアウイルスベクターの安全性 |
|
|
| 1.3.2. | その他 |
| 1.4. | 医療従事者への汚染 |
| 1.5. | 生殖細胞への遺伝子導入 |
| 1.6. | おわりに |
| 2. | リポソームの安全性 |
| 2.1. | はじめに |
| 2.2. | 培養細胞系でのカチオニックリポソームの細胞傷害性 |
| 2.3. | 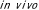 での安全性 での安全性 |
|
| |
| |
| 第7章 プロトコール-作成指針(症例付) |
 |
 |
|
 |
ADA欠損 |
|
| 1. | はじめに |
| 2. | アデノシンデアミナーゼ欠損症における遺伝子治療臨床研究の実施計画書 |
| 3. | 説明および同意書 |
|
|
| 4. | 北海道大学医学部附属病院の遺伝子治療臨床研究の実施計画に対する文部省厚生省の審査スケジェル |
|
| |
 |
AIDS |
|
| 1. | はじめに |
| 2. | プロトコール作成の経過 |
| 3. | 臨床治験としての遺伝子治療 |
|
|
|
| |
 |
腎癌 |
|
|
| 【参考資料】腎細胞癌に対する免疫遺伝子治療 |
‘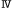 期腎細胞がん患者を対象とするGM-CSF遺伝子導入自己複製能喪失自家腫瘍細胞接種に関する臨床研究’束京大学医科学研究所附属病院 期腎細胞がん患者を対象とするGM-CSF遺伝子導入自己複製能喪失自家腫瘍細胞接種に関する臨床研究’束京大学医科学研究所附属病院 |
| |
 |
肺癌 |
|
| 1. | はじめに |
| 2. | 遺伝子治療臨床研究の名称 |
| 3. | 遺伝子治療臨床研究の目的 |
| 4. | 対象疾患およびその選定理由 |
| 4.1. | 非小細胞肺癌治療成績の現況 |
| 4.2. | 肺癌の分子生物学的特性 |
| 4.3. | 当該遺伝子治療臨床研究の概要 |
| 4.4. | 他の治療法との比較および遺伝子治療を選択した理由 |
| 5. | 遺伝子の種類およびその導入方法 |
| 5.1. | 癌抑制遺伝子p53の構造と性質 |
| 5.2. | アデノウイルスベクターを用いた遺伝子導入方法の概略および当導入法を選択した理由 |
| 5.3. | 正常型p53遺伝子発現アデノウイルスベクター(Ad5CMV p53)の作製方法と構造 |
| 6. | これまでの当該遺伝子治療臨床研究に関する培養細胞,実験動物を用いた研究成果 |
| 6.1. | 培養細胞を用いた研究の成果 |
| 6.1.1. | 培養細胞における遺伝子導入効率および導入された遺伝子の構造と安定性 |
| 6.1.2. | 培養細胞に導入された遺伝子の機能 |
| 6.1.3. | 培養細胞を用いた実験の評価 |
| 6.2. | 実験動物を用いた研究の成果 |
| 6.2.1. | 実験動物に導入された遺伝子の械能 |
| 6.2.2. | 動物実験の評価 |
| 7. | 安全性についての評価 |
| 7.1. | 遺伝子導入方法の安全性 |
| 7.1.1. | 遺伝子導入に用いるウイルスベクターの安全性 |
| 7.1.2. | 増殖性ウイルス出現の可能性 |
| 7.1.3. | 遺伝子導入に用いるウイルスベクターの細胞傷害性 |
| 7.1.4. | 患者以外の人への遺伝子導入の可能性 |
| 7.1.5. | 染色体内へ遺伝子が組み込まれる場合の問題点 |
|
|
| 7.1.6. | 癌原性の有無 |
| 7.2. | 遺伝子産物の安全性 |
| 8. | 遺伝子治療臨床研究の実施が可能であると判断する根拠 |
| 9. | 遺伝子治療臨床研究の実施計画 |
| 9.1. | 遺伝子治療臨床研究を含む全体の治療計画 |
| 9.2. | 被験者の選択基準および除外基準 |
| 9.2.1. | 選択基準 |
| 9.2.2. | 除外基準 |
| 9.3. | 被験者の同意の取得方法 |
| 9.4. | 実施期間および目標症例数 |
| 9.5. | 遺伝子治療臨床研究の実施方法(治療計画) |
| 9.5.1. | 対象群および治療群の設定 |
| 9.5.2. | 遺伝子導入方法 |
| 9.5.3. | CDDP投与 |
| 9.5.4. | 臨床検査項目および観察項目 |
| 9.5.5. | 副作用の判定基準 |
| 9.5.6. | 遺伝子治療臨床研究の評価方法,評価基準および中止判定基準 |
| 9.5.7. | 症例記録に関する記録用紙などの様式 |
| 9.5.8. | 記録の保存および成績の公表の方法 |
| 10. | 当該遺伝子治療臨床研究の実施施設の状況 |
| 11. | 当該遺伝子治療研究に関連する国内外の研究状況 |
| 11.1. | p53遺伝子治療および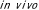 遺伝子治療に関する一般的な研究状況 遺伝子治療に関する一般的な研究状況 |
| 11.2. | 米国でのAd5CMV p53およびCDDPを用いた非小細胞肺癌の遺伝子治療の臨床データ |
| 12. | その他必要な事項〈正常型p53遺伝子発現アデノウイルスベクター(Ad5CMVp53)の供給,保管および品質管理〉 |
| 13. | 添付資料 |
| 14. | おわりに |
|
| |
| |
| 第8章 ガイドライン |
 |
 |
|
 |
厚生省,文部省遺伝子治療臨床研究のガイドラインについて |
|
| 1. | はじめに |
| 2. | 厚生省の厚生科学会議から出されたガイドライン |
| 2.1. | ガイドライン策定までの経緯 |
| 2.2. | ガイドラインの主な内容 |
| 3. | 文部省の学術審議会バイオサイエンス部会から出されたガイドライン |
|
|
| 4. | 厚生省薬務局から出された遺伝子治療用医薬品のガイドライン |
| 5. | 審査体制 |
| 6. | おわりに |
|
| |
 |
アメリカ・ヨーロッパ |
|
|
|
|
|
| |
| |
| 第9章 疾患モデル動物を用いた治療の実際 |
 |
 |
|
 |
発生工学による遺伝性疾患のモデルマウスの作製法 |
|
| 1. | はじめに |
| 2. | トランスジェニックマウス |
| 3. | ノックアウトマウス |
| 4. | 時期,部位特異的な変異導入法 |
|
|
| 4.1. | Cre-1oxPl組換え系 |
| 4.2. | Cre組換え酵素の発現 |
| 5. | おわりに |
|
| |
 |
発生関係モデルマウス |
|
| 1. | Fyn欠損マウス |
| 1.1. | Fynとは |
| 1.2. | Fyn欠損マウスの行動異常 |
| 1.3. | 情動因子としてのFyn分子機構の解析 |
| 1.4. | 学習異常 |
| 1.5. | Fyn結合分子の解析 |
| 1.6. | 新規カドヘリン型受容体 |
| 2. | ニューロトロフィンと受容体の欠損マウス |
| 2.1. | ニューロトロフィン |
| 2.2. | ニューロトロフィン遺伝子欠損マウス |
| 2.2.1. | NGF欠損マウス |
| 2.2.2. | BDNF欠損マウス |
| 2.2.3. | NT-3欠損マウス |
| 2.2.4. | NT-4/5欠損マウス |
| 2.3. | ニューロトロフィン受容体 |
| 2.4. | ニューロトロフィン受容体遺伝子欠損マウス |
| 2.4.1. | Trk欠損マウス |
| 2.4.2. | TrkB欠損マウス |
| 2.4.3. | TrkC欠損マウス |
| 2.4.4. | p75欠損マウス |
| 2.5. | 疾患との関連および今後の展望 |
| 3. | HLH型転写調節因子群欠損マウス |
|
|
| 3.1. | はじめに |
| 3.2. | MyoD,Myf5 |
| 3.3. | Myogenin |
| 3.4. | Mash1 |
| 3.5. | Math1 |
| 3.6. | Math2/Nex1 |
| 3.7. | NeuroD |
| 3.8. | Neurogenin |
| 3.9. | Hes1 |
| 4. | 神経特異的POU遺伝子変異マウス |
| 4.1. | はじめに |
| 4.2. | クラス POU転写因子の遺伝子欠損マウス POU転写因子の遺伝子欠損マウス |
| 4.2.1. | Brn-2欠損マウス |
| 4.2.2. | 0ct-6欠損マウス |
| 4.2.3. | Brn-4欠損マウス |
| 4.2.4. | Brn-1欠損マウス |
| 4.3. | クラス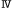 /POU転写因子の遺伝子欠損マウス /POU転写因子の遺伝子欠損マウス |
| 4.3.1. | Brn-3.1(Brn-3c)欠損マウス |
| 4.3.2. | Brn-3.2(Brn-3b)欠損マウス |
| 4.3.3. | Brn-3.0(Brn-3a)欠損マウス |
| 4.4. | おわりに |
|
| |
 |
神経関係モデルマウス |
|
| 1. | ミエリン形成障害マウス |
| 1.1. | 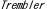 (Charcot-Marie-Tooth病)マウス (Charcot-Marie-Tooth病)マウス |
| 1.1.1. | はじめに |
| 1.1.2. | 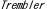 マウス マウス |
| 1.1.3. |  -Jマウス -Jマウス |
| 1.1.4. | Charcot-Marie-Tooth病タイプ1A |
| 1.1.5. | Charcot-Marie-Tooth病1BとⅩ |
| 1.1.6. | おわりに |
| 1.2. | quakingマウス |
| 1.2.1. | quakingマウスの病状と病理所見 |
| 1.2.2. | quakingマウスの生化学的異常―myelin-associated glycoproteinとの関連 |
| 1.2.3. | quakingマウスの遺伝子異常 |
| 1.3. |  マウス マウス |
| 1.3.1. | はじめに |
| 1.3.2. | PLP遺伝子の構造と遺伝子産物の機能 |
| 1.3.3. |  マウスにおける中枢神経系の異常 マウスにおける中枢神経系の異常 |
| 1.3.4. | 他のPLP遺伝子異常とオリゴデンドロサイトの細胞死 |
| 1.3.5. | PMDの疾患モデルとしてのPLPミュータント |
| 1.3.6. |  マウスにおける治療の試み マウスにおける治療の試み |
| 1.4. |  (シバラー)マウス (シバラー)マウス |
| 1.4.1. | 遺伝子変異 |
| 1.4.2. | 神経化学的変化 |
| 1.4.3. | 神経症状 |
| 1.4.4. | 組織学的変化 |
| 1.4.5. | 末梢神経系における変化 |
| 1.5. | 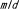 マウス-アンチセンスRNA産生マウス マウス-アンチセンスRNA産生マウス |
| 1.5.1. | 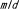 マウスにおけるミエリン塩基性蛋白質遺伝子の重複と逆位 マウスにおけるミエリン塩基性蛋白質遺伝子の重複と逆位 |
| 1.5.2. | ミエリン塩基性蛋白質遺伝子の再構成に伴うアンチセンスRNAの産生 |
| 1.5.3. | 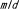 マウスにおけるミエリン塩基性蛋白質遺伝子の再構成機構 マウスにおけるミエリン塩基性蛋白質遺伝子の再構成機構 |
| 1.6. | twitcherマウス〈脳変性疾患の治療〉 |
| 2. | 脳のレセプター関係 |
| 2.1. | 代謝型グルタミン酸受容体欠損マウス |
| 2.1.1. | 背景 |
| 2.1.2. | ノックアウトマウスの所見 |
| 2.2. | NMDA受容体欠損マウス |
| 2.2.1. | ε1サブユニット欠損マウス |
|
|
| 2.2.2. | ε2サブユニット欠損マウス |
| 2.2.3. | ε3サブユニット欠損マウス |
| 2.2.4. | ε4サブユニット欠損マウス |
| 2.2.5. | ζ1サブユニット欠損マウス |
| 2.3. | アセチルコリン受容体欠損マウス |
| 2.3.1. | アセチルコリンレセプター |
| 2.3.2. | サブユニットの構造 |
| 2.3.3. | 神経性アセチルコリンレセプター |
| 2.3.4. | 各サブユニットの分布と構成 |
| 2.3.5. | アセチルコリンレセプターに関連した疾患 |
| 2.3.6. | ジーンターゲッティング |
| 2.4. | カテコールアミン関連酵素と受容体欠損マウス |
| 2.4.1. | はじめに |
| 2.4.2. | カテコールアミンによる神経伝達 |
| 2.4.3. | カテコールアミン合成系の欠損マウス |
| 2.4.4. | カテコールアミン分解酵素と輸送体の欠損マウス |
| 2.4.5. | カテコールアミン受容体の欠損マウス |
| 2.5. | ヒスタミン受容体欠損マウス |
| 2.5.1. | はじめに |
| 2.5.2. | ヒスタミンH1受容体遺伝子ノックアウトマウスの作製 |
| 2.5.3. | 中枢でのH1受容体の役割 |
| 2.5.4. | 考察 |
| 2.6. | タイプ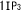 受容体欠損マウス 受容体欠損マウス |
| 2.6.1. | はじめに |
| 2.6.2. | 方法 |
| 2.6.3. | 結果 |
| 2.7. | グルタミン酸トランスポーター欠損マウス |
| 2.7.1. | グルタミン酸トランスポーターの概要 |
| 2.7.2. | GLT-1欠損マウスの作出 |
| 2.7.3. | GLT-1欠損マウスの表現型 |
| 2.7.4. | グルタミン酸興奮毒性個体モデルとしてのGLT-1欠損マウス |
| 2.7.5. | 他のグルタミン酸トランスポーター欠損マウス |
| 2.8. | ボンベシン受容体欠損マウス |
| 2.8.1. | ボンベシンシステムの概要 |
| 2.8.2. | BRS-3欠損マウス |
| 2.8.3. | GRP受容体欠損マウス |
| 2.8.4. | おわりに |
|
| |
 |
遺伝関係モデルマウス |
|
| 1. | フェニルケトン尿症 |
| 1.1. | フェニルケトン尿症とは |
| 1.2. | PKUのモデルマウス |
| 1.3. | PKUの遺伝子治療 |
| 1.4. | レトロウイルスベクターを用いた遺伝子導入 |
| 1.5. | アデノウイルスベクターを用いた遺伝子導入 |
| 1.6. | おわりに |
| 2. | 高チロシン血症モデルマウス |
| 2.1. | チロシン代謝障害の概要と分類 |
| 2.2. | 遺伝性高チロシン血症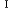 型(フマリルアセト酢酸分解酵素欠損症,hereditary tyrosinemiatypeI;HTI)(McKusik 276700) 型(フマリルアセト酢酸分解酵素欠損症,hereditary tyrosinemiatypeI;HTI)(McKusik 276700) |
| 2.2.1. | 臨床像 |
| 2.2.2. | 遺伝性高チロシン血症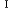 型(FAH欠損症)モデルマウス 型(FAH欠損症)モデルマウス |
| 2.2.3. | 遺伝性高チロシン血症 型(FAH欠損症)モデルマウスを用いた遺伝子治療実験 型(FAH欠損症)モデルマウスを用いた遺伝子治療実験 |
| 2.3. | 遺伝性高チロシン血症 型(4-ヒドロキシフェニルピルビン酸酸化酵素欠損症,hereditarytyrosinemia type 型(4-ヒドロキシフェニルピルビン酸酸化酵素欠損症,hereditarytyrosinemia type )(McKusik 276710) )(McKusik 276710) |
| 2.3.1. | 臨床像 |
| 2.3.2. | モデルマウス |
| 2.3.3. | モデルマウスを用いた遺伝子治療実験 |
| 2.4. | おわりに |
| 3. | ニーマンピック病 |
| 3.1. | はじめに |
| 3.2. | 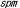 / /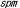 マウス マウス |
| 3.3. | 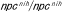 マウス マウス |
| 3.4. | ASMKOマウス |
| 3.5. |  マウス マウス |
| 3.6. | ニーマンピック病マウスの応用 |
| 4. | Krabbe病 |
| 4.1. | Krabbe病とは |
| 4.2. | 遺伝子治療の対象としての意義 |
| 4.3. | GALC遺伝子と遺伝子変異 |
| 4.4. | twitcherマウスの遺伝子治療モデル動物としての妥当性 |
| 4.5. | これまでの治療研究(造血幹細胞移植) |
| 4.6. | 遺伝子治療の試みと問題点 |
| 4.6.1. | レトロウイルスベクターの作製 |
| 4.6.2. | 遺伝子治療プロトコール |
| 4.6.3. | 結果 |
| 4.7. | 今後の展望 |
| 5. | 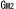 ガングリオシドーシス ガングリオシドーシス |
| 5.1. | はじめに |
| 5.2. | TSDモデルマウス |
| 5.3. | SDモデルマウス |
| 5.4. | 酵素活性化蛋白欠損症モデルマウス |
| 5.5. | 治療 |
| 5.5.1. | 骨髄移植 |
| 5.5.2. | ガングリオシド制限(substrate deprivation) |
| 5.5.3. | 神経細胞移植 |
| 5.5.4. | アデノウイルスを用いた遺伝子導入 |
| 5.6. | おわりに |
| 6. | Sly病 |
| 6.1. | はじめに |
| 6.2. | モデルマウスを用いた遺伝子治療の検討 |
| 6.2.1. | 造血細胞ヘレトロウイルスを用いて遺伝子治療を行った報告 |
| 6.2.2. | 培養皮膚線維芽細胞を用いたアプローチ |
| 6.2.3. | アデノウイルスによる 遺伝子治療 遺伝子治療 |
| 6.2.4. | アデノ随伴ウイルス(AAV)を用いた検討 |
| 6.2.5. | 中枢神経系への遺伝子治療 |
| 6.3. | おわりに |
| 7. | マスト細胞欠損マウス |
| 7.1. | Wマウス |
| 7.1.1. | はじめに |
| 7.1.2. |  ミュータントマウス ミュータントマウス |
| 7.1.3. |  - -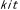 レセプターの構造およびその突然変異 レセプターの構造およびその突然変異 |
| 7.1.4. |  - -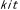 の模能獲得性突然変異 の模能獲得性突然変異 |
| 7.1.5. | おわりに |
| 7.2. | S マウス マウス |
| 7.2.1. | はじめに |
| 7.2.2. | S ミュータントマウスとSCFの構造 ミュータントマウスとSCFの構造 |
| 7.2.3. | SCFのマスト細胞における生理作用 |
| 7.2.4. | おわりに |
| 7.3. | アンギオテンシノーゲン遺伝子欠損マウス |
| 7.3.1. | はじめに |
| 7.3.2. | RA系 |
| 7.3.3. | アンギオテンシノーゲン遺伝子 |
| 7.3.4. | アンギオテンシノーゲン遺伝子欠損(agt-KO)マウス |
| 7.3.5. | RA系関連遺伝子欠損マウス |
| 8. | 糖尿病 |
| 8.1. | NIDDMマウス |
| 8.1.1. | はじめに |
| 8.1.2. | 自然発症モデルマウス |
| 8.1.3. | 遺伝子操作モデルマウス |
| 8.1.4. | おわりに |
| 8.2. | 糖尿病マウス,IDDMマウス,NODマウス |
| 8.2.1. | はじめに |
| 8.2.2. | Natural history |
| 8.2.3. | 遺伝因子 |
| 8.2.4. | 自己免疫機序による糖尿病発症機構 |
| 8.2.5. | 糖尿病発症過程における接着分子の役割 |
| 8.2.6. | おわりに |
| 9. | 筋ジストロフィー |
| 9.1. | 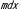 マウス マウス |
| 9.1.1. | 臨床,病理所見 |
| 9.1.2. | ジストロフィン欠損 |
| 9.1.3. | モデル動物としての有用性 |
| 9.2. | 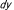 マウス マウス |
|
|
| 9.2.1. | はじめに |
| 9.2.2. | ラミニンの分子構造と遺伝子 |
| 9.2.3. | 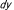 マウス, マウス,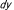 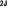 マウスにおけるラミニンα2鎖遺伝子異常 マウスにおけるラミニンα2鎖遺伝子異常 |
| 9.2.4. | ラミニンα2鎖遺伝子ノックアウトマウス |
| 9.2.5. | ラミニン欠損による先天性筋ジストロフィー |
| 9.2.6. | 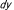 マウスへの筋芽細胞移植 マウスへの筋芽細胞移植 |
| 10. | ベージュマウス |
| 10.1. | はじめに |
| 10.2. | ベージュマウス |
| 10.3. | ベージュマウス,ベージュラットにおけるマスト細胞の異常 |
| 10.4. | ベージュ遺伝子,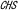 遺伝子 遺伝子 |
| 10.5. | おわりに |
| 11. | p53遺伝子欠損マウス |
| 11.1. | はじめに |
| 11.2. | p53の機能 |
| 11.3. | p53欠損マウスにおける自然発癌 |
| 11.4. | p53欠損マウスにおける発癌剤誘発発癌 |
| 11.4.1. | 7,12-ジメチルベンツアントラセン(DMBA)による皮膚発癌実験 |
| 11.4.2. | ジメチルニトロソアミン(DMN)による発癌実験 |
| 11.5. | Rb遺伝子との同時欠損 |
| 11.6. | p53欠損と細胞周期 |
| 11.7. | 個体形成異常 |
| 11.8. | おわりに |
| 12. | 家族性大腸腺腹症モデルマウス |
| 12.1. | はじめに |
| 12.2. | FAPモデルマウス |
| 12.3. | Minマウス(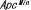 ) ) |
| 12.4. | Apc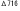 マウス マウス |
| 12.5. | Apc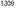 マウス マウス |
| 12.6. | Apc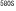 コンディショナルノックアウトマウス コンディショナルノックアウトマウス |
| 12.7. | 消化管腫瘍の発生を制御するmodifier遺伝子の同定Mom-1(modlfier of min-1) |
| 12.8. | おわりに |
| 13. | SAMマウス |
| 13.1. | 老化促進モデルマウス(SAM) |
| 13.2. | SAMの老化関連病態と発症機構 |
| 13.2.1. | 老年期脳機能障害 |
| 13.2.2. | 老年性骨粗鬆症 |
| 13.2.3. | 老年性アミロイド症 |
| 13.3. | 促進老化,老化病態の遺伝子治療のためのモデルマウスとしてのSAM |
| 13.4. | アデノウイルスベクターを用いたアミロイドーシスの遺伝子治療の試み |
| 13.5. | おわりに |
| 14. | ニーマンピック病C型モデルマウス |
| 14.1. | ヒトニーマンピック病C型とそのモデルマウス |
| 14.2. | モデルマウス臨床症状 |
| 14.3. | 生化学的所見 |
| 14.4. | 病理学的所見 |
| 14.5. | 治療への展望 |
| 15. | スフィンゴミエリナーゼ欠損マウス |
| 15.1. | はじめに |
| 15.2. | 作製法 |
| 15.3. | 臨床症状 |
| 15.4. | 生化学的所見 |
| 15.5. | 病理学的所見 |
| 15.6. | おわりに |
| 16. | メンケス病侯群(銅代謝異常)マウス |
| 16.1. | はじめに |
| 16.2. | 遺伝子異常 |
| 16.3. | 病態 |
| 16.4. | 症状,表現型 |
| 16.5. | 治療 |
| 16.6. | おわりに |
| 17. | OTC欠損マウス |
| 17.1. | はじめに |
| 17.2. | 0TC欠損モデルマウス |
| 17.2.1. | 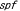 (sparse fur)mouse (sparse fur)mouse |
| 17.2.2. | 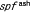 (sparse fur with abnormal skin and hair)mouse (sparse fur with abnormal skin and hair)mouse |
| 17.3. | アデノウイルスベクターを使ったOTC欠損マウスにおける遺伝子治療実験 |
| 17.4. | おわりに |
| 18. | その他 |
| 18.1. | ピルビン酸キナーゼ欠損マウス |
| 18.1.1. | はじめに |
| 18.1.2. | PK異常マウス |
| 18.1.3. | 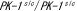 マウスの酵素学的特性 マウスの酵素学的特性 |
| 18.1.4. | PK遺伝子 |
| 18.1.5. | 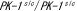 マウスヘの骨髄移植 マウスヘの骨髄移植 |
| 18.1.6. | 新生仔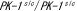 マウス マウス |
| 18.1.7. | おわりに |
| 18.2. | Gunnラット(Crigler-Najjar症候群Ⅰ型モデル動物) |
| 18.2.1. | はじめに |
| 18.2.2. | BR:UDP-glucuronosyltransferase |
| 18.2.3. | 遺伝性高BR血症治療モデルとしてのGunnラット |
| 18.3. | 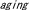 モデルマウス モデルマウス |
| 18.3.1. | はじめに |
| 18.3.2. | Klothoマウスに見られる老化 |
| 18.3.3. | 原因遺伝子;Klothoの同定 |
| 18.3.4. | Klotho発見の意義 |
| 18.4. | 自然発生アポE欠損高脂血症マウス |
| 18.4.1. | 高脂血症モデル動物の歴史と現状 |
| 18.4.2. | 自然発生アポE欠損高脂血症マウス |
| 18.4.3. | SHLマウスとアポEノックアウトマウスとの比較 |
| 18.4.4. | 今後の展望とモデルとしての可能性 |
| 18.4.5. | おわりに |
|
| |
 |
自己免疫疾患モデル |
|
| 1. | Xidマウス(免疫不全症マウス) |
| 1.1. | はじめに |
| 1.2. | XidマウスとB細胞異常 |
| 1.3. | Xidと疾患 |
| 1.3.1. | 感染症 |
| 1.3.2. | 自己免疫疾患 |
| 1.4. | XidとBtk異常 |
| 1.4.1. | XLAとBtk |
| 1.4.2. | XidとBtk |
| 1.4.3. | BtkとB細胞分化 |
| 1.5. | 遺伝子診断 |
| 1.6. | おわりに |
| 2. | SCIDマウス(重症複合免疫不全マウス) |
| 2.1. | はじめに |
| 2.2. | SCIDの免疫学的な所見 |
| 2.3. | SCIDの原因遺伝子発見 |
| 2.3.1. | SCIDの原因遺伝子 |
|
|
| 2.3.2. | XSCIDの原因遺伝子 |
| 2.4. | SCIDマウス |
| 3. | NZBマウス(自己免疫) |
| 3.1. | はじめに |
| 3.1.1. | NZBマウス |
| 3.1.2. | (NZB×NZW)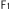 マウス(B/W マウス(B/W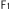 ) ) |
| 3.1.3. | NZB/KNマウス |
| 4. | MRL/ マウス(自己免疫) マウス(自己免疫) |
| 4.1. | はじめに |
| 4.2. | MRL/Mp-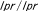 (MRL/ (MRL/ )マウス )マウス |
| 4.3. | MRL/Mp-+/+(MRL/n)マウス |
| 5. | lprマウス |
| 5.1. | 分子遺伝学 |
| 5.2. | FasとFasLのcDNA |
| 5.3. | 背景遺伝子と自己免疫病 |
| 5.4. | 発病のメカニズム |
| 5.5. | 遺伝子操作による病態の軽減と遺伝子治療 |
|
| |
 |
霊長類モデル動物 |
|
| 1. | アカゲザル |
| 1.1. | はじめに |
| 1.2. | 安全性 |
| 1.3. | 遺伝性疾患 |
| 1.4. | 神経性疾患 |
| 1.5. | 血液疾患 |
| 1.5.1. | サルを用いる実験の必要性 |
| 1.5.2. | 造血幹細胞に対する遺伝子導入 |
| 1.5.3. | リンパ球に対する遺伝子導入 |
|
|
| 1.6. | 感染症 |
| 1.7. | おわりに |
| 2. | 遺伝子治療前臨床試験動物としての小型霊長類コモンマーモセット |
| 2.1. | はじめに |
| 2.2. | コモンマーモセットについて |
| 2.3. | マーモセット造血幹細胞への遺伝子導入の検討 |
| 2.4. | おわりに |
|
| |