 |
 |
| 出版にあたって |
| |
| 第1章 総論 |
 |
 |
|
| はじめに |
| |
 |
天然脂質と人工脂質 |
|
| 1.1. | 生体膜の構造と機能 |
| 1.2. | 生体膜の構成成分 |
| 1.3. | 天然脂質の分子構造 |
| 1.4. | 脂質の会合構造 |
|
|
| 1.5. | 脂質会合体の動的挙動 |
| 1.6. | リポソーム |
| 1.7. | 合成脂質二分子膜 |
| 1.8. | 脂質分子集合体の利用 |
|
| |
 |
天然酵素と人工酵素 |
|
| 2.1. | 化学工業プロセスの現状と未来像 |
| 2.2. | バイオテクノロジーにおける酵素の役割 |
|
|
| 2.3. | 天然酵素の機能 |
| 2.4. | 天然酵素の利用とその限界 |
|
| |
 |
人工酵素開発へのアプローチ |
|
|
|
|
|
| |
| |
| 第2章 超分子素子の設計と合成 |
 |
 |
|
 |
合成ペプチド脂質 |
|
| 1.1. | 分子設計の基本概念 |
| 1.2. | カチオン性脂質 |
| 1.3. | アニオン性脂質 |
|
|
| 1.4. | 双性イオン型脂質 |
| 1.5. | 非イオン性脂質 |
| 1.6. | 軸不斉部位をもつ脂質 |
|
| |
 |
マクロ環化合物 |
|
| 2.1. | 分子設計の基本概念 |
| 2.2. | タコ形シクロファン |
| 2.2.1. | タコ形シクロファンの合成 |
| 2.3. | ヘキサパスシクロファンとその金属錯体 |
|
|
| 2.3.1. | ヘキサパスシクロファン |
| 2.3.2. | シクロファン系金属錯体 |
| 2.4. | ステロイドシクロファン |
| 2.5. | かご型シクロファン |
|
| |
 |
捕酵素誘導体 |
|
| 3.1. | 分子設計の基本概念 |
| 3.2. | ニコチンアミド誘導体 |
| 3.3. | ビタミンB 誘導体 誘導体 |
| 3.4. | 単純ビタミンB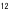 モデル錯体 モデル錯体 |
| 3.5. | 疎水性ビタミンB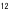 モデル錯体 モデル錯体 |
|
|
| 3.5.1. | 単純型疎水性ビタミンB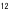 (Cob7Cnester) (Cob7Cnester) |
| 3.5.2. | ビナフチル基を有する疎水性ビタミンB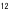 |
| 3.5.3. | ストラップ型疎水性ビタミンB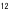 |
| 3.5.4. | 脂質に結合した疎水性ビタミンB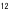 |
|
| |
| |
| 第3章 ペプチド脂質の会合形態と動的挙動 |
 |
 |
|
 |
脂質分子集合体の物理的評価法 |
|
| 1.1. | 電子顕微鏡観察 |
| 1.1.1. | ネガティブ染色法 |
| 1.1.2. | フリーズフラクチャーレプリカ法 |
| 1.1.3. | 制限視野電子線回折法 |
| 1.2. | Ⅹ線回折法 |
| 1.3. | NMR法 |
| 1.3.1. | 基礎理論 |
| 1.3.2. | 実験の手順と注意 |
| 1.3.3. | 膜の流動性の評価 |
| 1.3.4. | 膜透過現象の解析への応用 |
|
|
| 1.4. | ESR法 |
| 1.4.1. | ESRの原理 |
| 1.4.2. | スピントラップ法 |
| 1.4.3. | スピンラベル法 |
| 1.5. | 光散乱法 |
| 1.5.1. | 動的光散乱法 |
| 1.5.2. | 静的光散乱法 |
| 1.6. | 示差走査熱量分析法 |
| 1.7. | 蛍光偏光法 |
|
| |
 |
ペプチド脂質の会合構造 |
|
| 2.1. | イオン性ペプチド脂質 |
| 2.1.1. | カチオン性脂質 |
| 2.1.2. | アニオン性脂質 |
| 2.1.3. | 双性イオン型脂質 |
| 2.2. | 非イオン性ペプチド脂質 |
|
|
| 2.3. | ペプチド脂質混合系 |
| 2.3.1. | ラメラ相を形成する脂質混合系 |
| 2.3.2. | 立方体相を形成する脂質混合系 |
| 2.3.3. | ヘキサゴナル相を形成する脂質混合系 |
| 2.4. | 分子構造と会合構造との関係 |
|
| |
 |
ペプチド脂質会合体の相転移挙動 |
|
| 3.1. | イオン性脂質 |
| 3.1.1. | 示差走査熱量分析法による検討 |
| 3.1.2. | 蛍光偏光法による検討 |
|
|
| 3.2. | 非イオン性脂質 |
| 3.3. | 脂質混合系 |
| 3.4. | 相転移パラメータ一覧 |
|
| |
 |
二分子膜ベシクルの動的挙動 |
|
| 4.1. | 会合形態の物理・化学的安定性 |
| 4.1.1. | ペプチド脂質の化学的安定性 |
| 4.1.2. | 単一膜ベシクルの物理的安定性 |
| 4.2. | ベシクル間の脂質交換 |
| 4.2.1. | スピンラベル化脂質の合成 |
| 4.2.2. | 脂質交換速度の測定 |
|
|
| 4.3. | フリップ・フロップ |
| 4.4. | 物質透過性 |
| 4.4.1. | 水溶性アニオン性物質の透過 |
| 4.4.2. | 水溶性カナオン性物質の透過 |
| 4.5. | 膜融合能 |
| 4.6. | ベシクルパラメータ |
|
| |
 |
非二分子膜構造が関与する膜間相互作用 |
|
| 5.1. | イオン性及び非イオン性ペプチド脂質の膜間相互作用 |
| 5.2. | 非イオン性ペプチド脂質が誘起する膜融合 |
|
|
| 5.3. | 非二分子膜構造を経由する膜融合 |
| 5.4. | 水溶性高分子が誘起する膜融合 |
|
| |
| |
| 第4章 超分子への組織化とミクロ環境評価 |
 |
 |
|
 |
ペプチド脂質とマクロ環化合物 |
|
| 1.1. | ハイブリッド分子集合体の調製 |
| 1.2. | マクロ環化合物の固定化率 |
| 1.3. | ゲル-液晶相転移 |
|
|
| 1.4. | 会合体の平均粒径 |
| 1.5. | マクロ環化合物の微視的環境 |
| 1.6. | 蛍光プローブ法による膜の流動性の検討 |
|
| |
 |
ペプチド脂質とビタミンB 誘導体 誘導体 |
|
| 2.1. | ビタミンB 人工ホロ酵素の構成 人工ホロ酵素の構成 |
| 2.2. | ビタミンB 人工酵素の活性部位のミクロ環境 人工酵素の活性部位のミクロ環境 |
| 2.2.1. | アミノ酸残基の酸解離挙動 |
|
|
| 2.2.2. | ビタミンB 部位の酸解離挙動 部位の酸解離挙動 |
| 2.2.3. | ビタミンB 部位のミクロ極性 部位のミクロ極性 |
| 2.2.4. | ビタミンB 部位の分子運動性 部位の分子運動性 |
|
| |
 |
ペプチド脂質及びアザパラシクロファンとビタミンB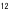 誘導体 誘導体 |
|
| 3.1. |  , , '-ジドデシル-N '-ジドデシル-N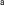 -(6-トリメチルアンモニオヘキサノイル)-L-アラニンアミドブロミド( -(6-トリメチルアンモニオヘキサノイル)-L-アラニンアミドブロミド(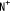 C C Ala2C Ala2C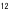 )の単一層二分子膜ベシクルによる疎水性ビタミンB )の単一層二分子膜ベシクルによる疎水性ビタミンB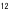 類の取り込み挙動 類の取り込み挙動 |
| 3.1.1. | ゲルクロマトグラフ法による取り込み挙動の検討 |
| 3.1.2. | 電子スペクトルによる取り込み場の評価 |
| 3.1.3. | 二分子膜ベシクルの電子顕微鏡観察 |
| 3.2. |  , , -ジドデシル-N -ジドデシル-N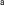 -(6-トリメチルアンモニオヘキサノイル)-L-ヒスチジンアミドブロミド( -(6-トリメチルアンモニオヘキサノイル)-L-ヒスチジンアミドブロミド(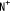 C C His2C His2C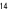 )の単一層二分子膜ベシクルによる疎水性ビタミンB )の単一層二分子膜ベシクルによる疎水性ビタミンB 類の取り込み挙動 類の取り込み挙動 |
|
|
| 3.3. |  , , ', ', '', '', ''',-テトラキス[2-[N-[1- ''',-テトラキス[2-[N-[1- , , -ジテトラデシルカルバモイル]-2-〔6-(トリメチルアンモニオ)ペンタカルボキサミド〕-5-ペンチル]カルバモイル]エチル]-3,10,21,28-テトラオキソ-2,1l,20,29-テトラアザ[3,3,3,3]パラシクロファンテトラブロミド(OC[C -ジテトラデシルカルバモイル]-2-〔6-(トリメチルアンモニオ)ペンタカルボキサミド〕-5-ペンチル]カルバモイル]エチル]-3,10,21,28-テトラオキソ-2,1l,20,29-テトラアザ[3,3,3,3]パラシクロファンテトラブロミド(OC[C LysC LysC N+])2C N+])2C ] ] )による疎水性ビタミンB )による疎水性ビタミンB 類の取り込み挙動 類の取り込み挙動 |
| 3.4. | 蛍光プローブによる取り込み部位の評価 |
|
| |
 |
二本鎖脂質と一本鎖脂質 |
|
| 4.1. | ミセル、ベシクル、ハイブリッド型分子集合体のミクロ環境 |
| 4.1.1. | 蛍光スペクトル法によるミクロ環境評価 |
| 4.1.2. | 電子顕微鏡観察 |
|
|
| 4.1.3. | 動的光散乱法による分子集合体の観察 |
| 4.2. | 超分子集合体への組織化とイオン強度 |
|
| |
| |
| 第5章 人工レセプター |
 |
 |
|
 |
分子認識能の評価法 |
|
| 1.1. | 蛍光スペクトル法 |
| 1.2. | NMRスペクトル法 |
|
|
| 1.3. | 電子スペクトル及び円二色性(CD)スペクトル法 |
|
| |
 |
水中の分子認識能 |
|
| 2.1. | タコ形シクロファン |
| 2.1.1. | 分子認識能 |
| 2.1.2. | 微視的環境 |
| 2.1.3. | 包接形態 |
| 2.2. | ヘキサパスシクロファン |
| 2.2.1. | ヘキサパスシクロファンのゲスト分子包接機能 |
| 2.2.2. | ヘキサパスシクロファン金属錯体のゲスト分子包接機能 |
|
|
| 2.3. | ステロイドシクロファン |
| 2.4. | かご型シクロファン |
| 2.4.1. | Kyuphane分子認識能 |
| 2.4.2. | 不斉なゲスト取り込み部位の構成 |
| 2.4.3. | 熱力学的パラメータ |
| 2.4.4. | 誘起CDスペクトル |
| 2.4.5. | 生理活性物質に対する分子識別 |
| 2.4.6. | ビリルビンに対する不斉認識 |
|
| |
 |
二分子膜中の分子認識能 |
|
| 3.1. | タコ形シクロファンとステロイドシクロファン |
| 3.2. | ヘキサパスシクロファン |
| 3.2.1. | シデロフォアとそのモデル |
| 3.2.2. | ヘキサパスシクロファンと二分子膜の相互作用 |
|
|
| 3.2.3. | 二分子膜中への鉄(Ⅲ)イオン取り込み挙動 |
| 3.3. | かご型シクロファン |
| 3.3.1. | 色素類に対する分子認識 |
| 3.3.2. | アミノ酸類に対する分子認識 |
|
| |
| |
| 第6章 人工加水分解酵素 |
 |
 |
|
 |
加水分解酵素のモデル化 |
|
| |
 |
動力学解析法 |
|
| |
 |
タコ形アザパラシクロファン |
|
| 3.1. | はじめに |
| 3.2. | タコ形アザパラシクロファンの合成 |
| 3.3. | 基質取り込み能 |
| 3.4. | 会合挙動 |
|
|
| 3.5. | 加水分解触媒機能 |
| 3.5.1. | 基質選択性 |
| 3.5.2. | 反応機構 |
|
| |
 |
一本鎖ペプチド脂質(ミセル系) |
|
| 4.1. | 一本鎖ペプチド脂質の誕生 |
| 4.2. | ミセルの構造とミセル動力学 |
| 4.2.1. | ミセルの構造 |
| 4.2.2. | ミセル動力学 |
| 4.3. | 人工チオプロテアーゼ |
| 4.3.1. | はじめに |
| 4.3.2. | アニオン性単独ミセル系 |
| 4.3.3. | カチオン性混合ミセル系 |
| 4.3.4. | カチオン性単独ミセル系 |
| 4.4. | 人工セリンプロテアーゼ |
|
|
| 4.4.1. | はじめに |
| 4.4.2. | モデル脂質の構造 |
| 4.4.3. | 混合ミセル系での触媒活性 |
| 4.4.4. | 中性イミダゾール基の反応性 |
| 4.4.5. | 重水素同位体効果 |
| 4.4.6. | 一般塩基触媒に対する動力学的根拠 |
| 4.4.7. | 一般塩基触媒の比率 |
| 4.4.8. | 反応場の効果 |
| 4.4.9. | セリンプロテアーゼの三つ組(Triad)との機構類似性 |
|
| |
 |
二本鎖ペプチド脂質(二分子膜系) |
|
| 5.1. | ミセル反応場の評価 |
| 5.1.1. | 会合体の構造 |
|
|
| 5.1.2. | ミセルのミクロ環境 |
| 5.2. | 二本鎖ペプチド脂質の誕生 |
|
| |
 |
不斉選択性 |
|
| 6.1. | はじめに |
| 6.2. | ミセル系 |
| 6.2.1. | 研究の背景 |
| 6.2.2. | 混合ミセル系 |
| 6.2.3. | 高次ミセル系エステラーゼモデルの構築 |
| 6.2.4. | 界面活性剤の濃度効果 |
| 6.3. | 二分子膜ベシクル系 |
| 6.3.1. | 基質結合親和性 |
|
|
| 6.3.2. | 温度制御 |
| 6.3.3. | エントロピー効果 |
| 6.4. | ハイブリッド型分子集合体系 |
| 6.4.1. | 膜組成変化による立体制御 |
| 6.4.2. | 酵素に匹敵する立体制御の発現 |
| 6.4.3. | 不斉識別機構 |
| 6.5. | おわりに |
|
| |
| |
| 第7章 NADH人工酵素 |
 |
 |
|
| はじめに |
| |
 |
天然のNADH酵素 |
|
| 1.1. | NADH酵素の生化学的機能 |
| 1.2. | 補酵素の化学的性質 |
|
|
|
| |
 |
人工デヒドロゲナーゼ |
|
| 2.1. | NADHのモデル研究 |
| 2.1.1. | 反応活性化 |
| 2.1.2. | 不斉選択性 |
| 2.2. | 二分子膜型人工酵素 |
|
|
| 2.2.1. | 会合挙動 |
| 2.2.2. | 分子認識能 |
| 2.2.3. | 還元反応活性 |
|
| |
| |
|
|
 |
天然のビタミンB 酵素 酵素 |
|
| 1.1. | ビタミンB 酵素の生化学的機能 酵素の生化学的機能 |
| 1.2. | 補酵素の化学的性質 |
|
|
| 1.3. | ビタミンB 酵素の反応機構 酵素の反応機構 |
| 1.4. | アポタンパクの構造と機能 |
|
| |
 |
人工アミノトランスフェラーゼ |
|
| 2.1. | アミノ基転移反応のモデル研究 |
| 2.1.1. | 補酵素自体の機能に着目したモデル研究 |
| 2.1.2. | アポ酵素の分子認識能に着目したモデル研究 |
| 2.2. | 二分子膜型人工酵素 |
|
|
| 2.2.1. | Schiff塩基生成挙動 |
| 2.2.2. | α-ケト酸からα-アミノ酸への変換 |
| 2.2.3. | α-アミノ酸からα-ケト酸への変換 |
| 2.2.4. | 完全サイクル型アミノ基転移反応 |
|
| |
 |
人工トリプトファンシンターゼ |
|
| 3.1. | α-置換反応のモデル研究 |
| 3.2. | 二分子膜型人工酵素 |
| 3.2.1. | 触媒活性 |
|
|
|
| |
 |
人工アルドラーゼ |
|
| 4.1. | アルドラーゼ型反応のモデル研究 |
| 4.2. | 二分子膜型人工酵素 |
|
|
|
| |
| |
|
|
 |
天然のビタミンB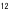 酵素 酵素 |
|
| 1.1. | ビタミンB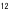 補酵素の構造と役割 補酵素の構造と役割 |
| 1.2. | アデノシルコバラミンが関与する酵素反応の機構 |
| 1.3. | Co-C結合の活性化とアポ酵素の役割 |
|
|
| 1.4. | 補酵素B のCo-C結合の開裂様式及びモデル反応 のCo-C結合の開裂様式及びモデル反応 |
| 1.5. | ビタミンB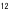 モデル錯体 モデル錯体 |
|
| |
 |
ビタミンB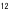 人工酵素 人工酵素 |
|
| 2.1. | メチルマロニル-CoAムターゼのモデル反応 |
| 2.1.1. | アルキル錯体の合成 |
| 2.1.2. | モデル反応における反応場の効果 |
| 2.1.3. | モデル反応に及ぼすコバルトの効果 |
| 2.2. | グルタミン酸ムターゼのモデル反応 |
| 2.2.1. | アルキル錯体の合成 |
| 2.2.2. | モデル反応における反応場の効果 |
| 2.2.3. | グルタミン酸ムターゼのモデル反応における転位基の選択性 |
| 2.2.4. | モデル反応に及ぼすコバルトの効果 |
| 2.3. | 反応機構の研究方法 |
|
|
| 2.3.1. | 電子スペクトルによる反応の追跡 |
| 2.3.2. | 電子スピン共鳴スペクトルによる反応の追跡 |
| 2.3.3. | 二本鎖ペプチド脂質(N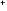 C C Ala2C Ala2C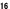 )及びアザパラシクロファン(OC[C )及びアザパラシクロファン(OC[C Lys(C Lys(C N N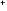 )2C )2C ] ] )の濃度依存性 )の濃度依存性 |
| 2.3.4. | 塩化第二銅(CuCl )添加効果 )添加効果 |
| 2.3.5. | 蛍光プローブによる反応場の評価 |
| 2.3.6. | ベンゼン中における生成物の温度変化 |
| 2.4. | 反応機構 |
| 2.5. | まとめ |
|
| |
 |
基質の活性化を伴う異性化反応 |
|
| 3.1. | メチルマロニル-CoAムターゼのモデル反応 |
| 3.2. | グルタミン酸ムターゼのモデル反応 |
| 3.3. | 環拡大反応 |
|
|
|
| |
| |
| 第10章 将来の展望 |
 |
 |
|
| 付録化合物一覧 |
| |
| 1. | 合成ペプチド脂質 |
| 1.1. | 一本ペプチド界面活性剤 |
| 1.2. | カチオン性ペプチド脂質 |
| 1.3. | アニオン性ペプチド脂質 |
| 1.4. | 双性イオン型ペプチド脂質 |
| 1.5. | 非イオン型ペプチド脂質 |
| 1.6. | 軸不斉部位をもつペプチド脂質 |
| 2. | マクロ環化合物 |
| 2.1. | 単環性シクロファン |
|
|
| 2.2. | タコ形シクロファン |
| 2.3. | ヘキサパスシクロファン |
| 2.4. | ステロイドシクロファン |
| 2.5. | かご型シクロファン |
| 3. | 補酵素誘導体 |
| 3.1. | NADH誘導体 |
| 3.2. | ビタミンB 誘導体 誘導体 |
| 3.3. | ビタミンB 誘導体 誘導体 |
|
| |